Aérosolthérapie : Un modèle de poumons ex-vivo
Jérémie Pourchez est chercheur en Ingénierie pour la Santé à Mines Saint-Étienne. Il y développe, avec ses collègues médecins du CHU de Saint-Étienne, un modèle de poumons ex-vivo permettant d’améliorer les performances des dispositifs médicaux d’aérosolthérapie. L’avantage de cette méthode ? Évaluer les thérapies inhalées en limitant le recours à l’expérimentation animale.
[box type= »shadow » align= » » class= » » width= » »]Cet article fait partie de notre dossier Quand l’ingénierie se met au service de la santé. [/box]
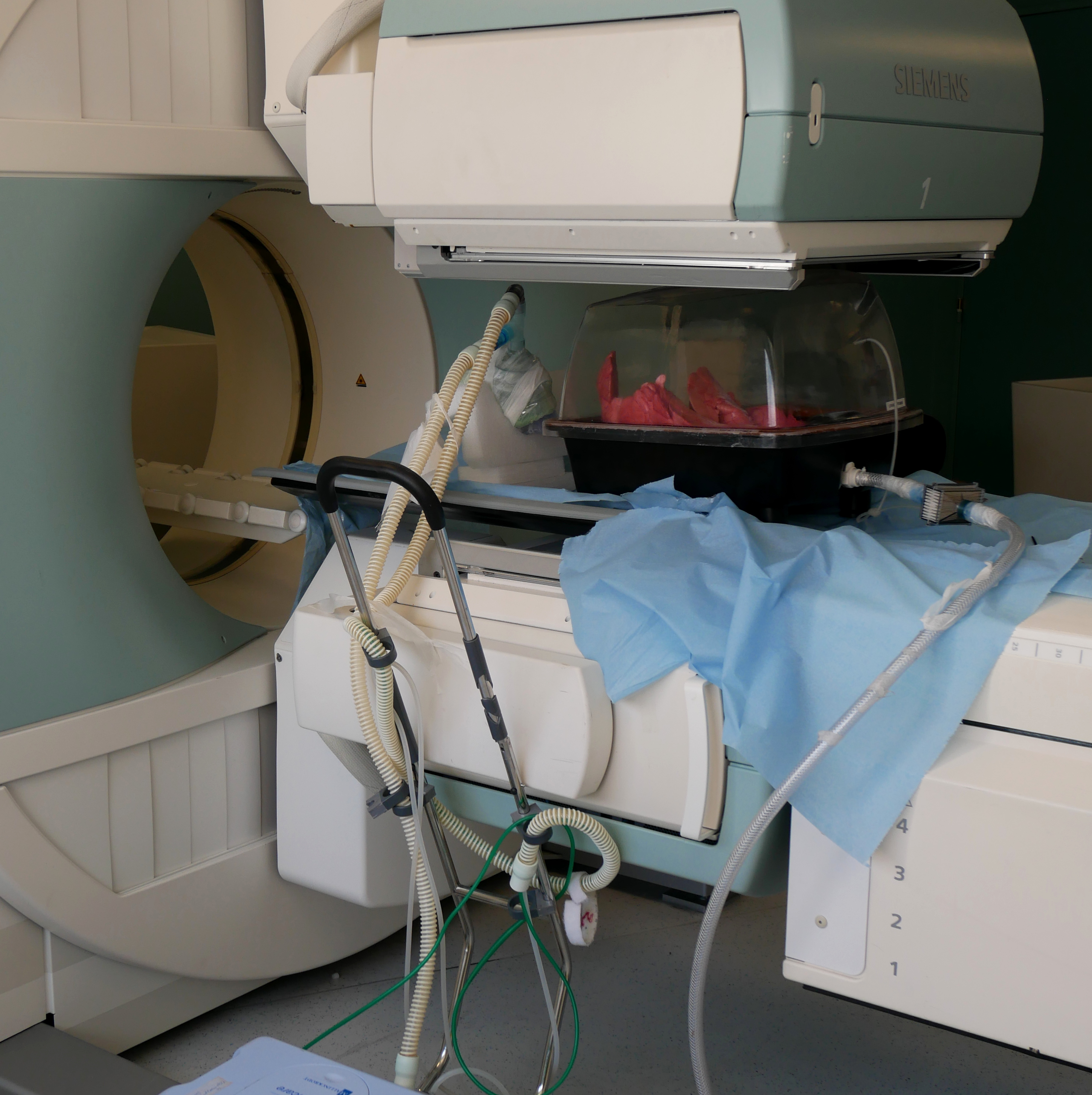
Imaginez. Sur une paillasse de laboratoire, une tête humaine réalisée par impression 3D. Cette réplique anatomique est reliée par un tuyau mimant la trachée à une enceinte sous vide. À l’intérieur, des poumons. Périodiquement, une pompe simule la dépression qui se crée naturellement dans la cage thoracique pour induire la respiration. Le poumon se gonfle et se dégonfle. Ce modèle physique de l’appareil respiratoire est bien réel. Il se trouve au Centre Ingénierie Santé de Mines Saint-Étienne, et il est développé par l’équipe de Jérémie Pourchez, spécialiste des particules inhalées et de l’aérosolthérapie.
Dans le cadre du projet ANR AMADEUS, les chercheurs stéphanois développent ce modèle de poumons ex-vivo pour simuler la respiration et les pathologies pouvant y être associées comme l’asthme ou la fibrose. Deux versions ont déjà étés développées, une de taille adulte, une autre de taille enfant. Depuis deux ans, ils travaillent au développement et à la validation de ce modèle. Grâce à lui, ils peuvent étudier la délivrance de médicaments par aérosolthérapie en offrant une solution alternative et moins coûteuse que l’expérimentation animale. Le modèle pulmonaire ex vivo est en effet éthiquement préférable, les organes utilisés provenant uniquement de déchets issus des abattoirs pour l’alimentation humaine.
Un modèle de poumons ex vivo vaut-il des poumons réels ?
Pour les chercheurs, l’un des objectifs est de démontrer que ces modèles ex vivo sont pertinents en terme de prédiction par rapport à ce qui se passe in vivo chez l’être humain. Cela implique trois points à aborder.
En premier lieu, il faut étudier la physiologie respiratoire des modèles. Cela se fait grâce aux mêmes capteurs que ceux utilisés chez l’être humain — pour mesurer les paramètres respiratoires d’un asthmatique par exemple. Il faut alors montrer que les paramètres du modèle correspondent aux paramètres de l’être humain. Il faut ensuite analyser la ventilation du modèle, c’est-à-dire s’assurer qu’il n’y a pas d’obstacle dans les bronches. Pour cela les poumons ex vivo respirent un gaz radioactif — du krypton — utilisé comme traceur pour visualiser la ventilation dans l’ensemble du modèle. La dernière étape est l’étude du dépôt d’aérosol dans les voies respiratoires : où se déposent les particules inhalées lorsqu’on utilise un nébuliseur ou un spray ? Là aussi, cela se fait grâce à un radiomarquage permettant d’observer le dépôt d’aérosols par imagerie en médecine nucléaire.
Les résultats sont alors comparés à ceux connus chez l’humain dans la littérature scientifique. Si les paramètres correspondent, le modèle est validé. Seul problème : les poumons de porc récupérés dans les abattoirs correspondent aux poumons d’une personne saine. Or, le but de ces recherches est de mettre au point un modèle pouvant mimer les pathologies pulmonaires pour tester l’efficacité de traitements en aérosolthérapie.
Du modèle sain au modèle pathologique
Il existe différentes pathologies pouvant porter atteinte aux capacités respiratoires, et la pollution présente dans l’air a tendance à augmenter leur fréquence d’apparition. La fibrose, par exemple, dénature les fibres élastiques permettant à nos poumons de se gonfler lors de l’inspiration. Le poumon est alors plus rigide, et la respiration difficile. Pour changer l’élasticité des poumons ex vivo ils sont traités thermiquement, à la vapeur, pour rigidifier la surface du tissu et mimer le comportement mécanique des poumons humains atteints de fibrose.
D’autres pathologies, comme la mucoviscidose, se concrétisent entre autres, par des sécrétions dans les poumons gênant le passage de l’air dans les bronches. Les chercheurs vont alors insérer dans le poumon-modèle des sécrétions artificielles à base d’agents épaississants mimant ces difficultés.
Futures évolutions du modèle
Imiter ces pathologies est une première étape indispensable. Mais pour étudier la capacité d’action des traitements d’aérosolthérapie, il faut aussi évaluer leur diffusion dans le sang qui peut être un avantage ou un inconvénient. En effet, le poumon est aussi une porte d’entrée permettant au médicament de se propager dans le corps. L’équipe de chercheurs a donc installé un dernier outil : une pompe simulant les battements de notre cœur. « Grâce à cette pompe, un fluide circule dans le modèle comme le sang circule dans les poumons d’un être humain » indique Jérémie Pourchez. « Lors d’un test, il est alors possible de mesurer la quantité de médicament inhalé qui va se diffuser dans le fluide. Actuellement, nous travaillons à la validation de ce modèle amélioré ».
Un enjeu est le développement de traitements systémiques par inhalation, c’est-à-dire des traitements destinés à traiter des organes autres que les poumons en utilisant la voie inhalée et les poumons comme porte d’entrée dans l’organisme. « Il y a quelques années, de l’insuline sous forme de spray a été mise sur le marché » cite par exemple Jérémie Pourchez. L’insuline, utilisée pour traiter le diabète, nécessite des injections régulières. « Pour le patient, ce serait une alternative soulageante de remplacer ces injections par des inhalations. Mais c’est également un médicament qui nécessite une dose extrêmement précise du principe actif, et obtenir cette dose d’insuline très précise par aérosol reste un challenge scientifique et technique ».
L’avantage d’un traitement par voie inhalée, au-delà de la simplicité d’utilisation, est la rapidité avec laquelle le principe actif peut se retrouver dans le sang. « C’est pour cela que la cigarette électronique fonctionne mieux qu’un patch pour délivrer de la nicotine et satisfaire le manque lors de tentatives d’arrêt du tabac » souligne le chercheur. La dose de nicotine transmise se dépose dans les poumons et est directement diffusée dans le sang. « Cela m’a également amené à étudier les dispositifs de type cigarette électronique pour évaluer leur capacité à délivrer différents médicaments par aérosol » explique Jérémie Pourchez.
En modifiant certains aspects techniques, ces dispositifs pourraient devenir des outils d’aérosolthérapie, et être utilisés dans le futur pour soigner certaines pathologies pulmonaires. C’est un des projets en cours de l’équipe stéphanoise, mais il nécessite encore des recherches conséquentes au niveau de la toxicité potentielle du dispositif et de son efficacité en fonction des médicaments inhalés testés. Plutôt que de servir uniquement d’outil pour le sevrage tabagique, la cigarette électronique pourrait donc un jour devenir une nouvelle technologie de traitement médical par aérosol.
Enfin, ce modèle permettra également de répondre à une autre problématique centrale dans le cadre de la transplantation pulmonaire. Lors d’un don d’organe, c’est à l’agence de biomédecine que revient la décision de proposer éventuellement ce don aux équipes de greffe. Mais cette décision d’urgence peut se baser sur des paramètres parfois insuffisants pour évaluer à distance la réelle qualité du greffon. « Par exemple, pour évaluer la qualité du poumon d’un donneur », précise Jérémie Pourchez, « on se réfère à des données importantes telles que : le tabagisme, l’âge, ou les pathologies connues du donneur. Notre dispositif expérimental servant à faire respirer les poumons ex vivo peut alors servir d’outil afin d’objectiver plus précisément la qualité de poumons lors de sa réception par l’équipe de greffe, et de déterminer s’il est pertinent de réaliser la transplantation à partir de mesures réalisées sur l’organe à greffer ».









Trackbacks (rétroliens) & Pingbacks
[…] Aérosolthérapie : Un modèle de poumons ex-vivo […]
Laisser un commentaire
Rejoindre la discussion?N’hésitez pas à contribuer !